水 の密度(黒い線)
二酸化炭素の密度(青い線)
二酸化炭素ハイドレートの密度(赤い線)
ガスをどのようにして貯蔵するのですか?
地球温暖化に関する原因物質の一つとされている二酸化炭素について考えてみましょう。現在,電力会社などを中心として火力発電所などから排出される排煙中の二酸化炭素を回収する技術開発が進められています(電力会社等エネルギー転換部門は,日本国内の総排出量の30から40%をしめる)。火力発電所から排出される二酸化炭素の量は,石炭火力発電所で0.975 kg-CO2/kWh,石油火力で0.742 kg-CO2/kWh,LNG(液化天然ガス)火力で0.608 kg-CO2/kWh(電力中央研究所報告書より)であり,日本の発電所から排出される二酸化炭素は年間3億1050万トン!!!(電力中央研究所報告書より)単純計算で一日80万トンもの膨大な量を排出しています。もちろん,これら全てを回収する必要はありません。しかし排出二酸化炭素の数割を回収したとしても,その量は膨大であり,効率の良い処理(利用)方法が開発されるまでは,二酸化炭素を貯蔵する必要がでてきます。我々は,この貯蔵に関して,自然の力を利用できないだろうか?と考えています。
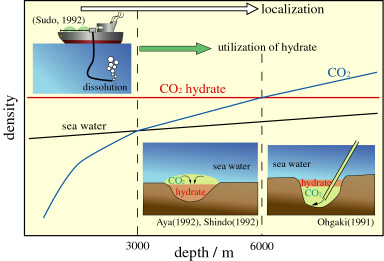
| 右図は,海を利用した二酸化炭素の隔離(一部は貯留)方法を,利用する海の深さと海水や二酸化炭素,二酸化炭素ハイドレートの密度との関係で示しています。我々が提案しているのは,右図の1番右側の深度6,000 m以上の海底を利用する方法です。自然の力を利用すると書きましたが,具体的には二酸化炭素ハイドレートを利用します(ハイドレートに関しては,こちらを御覧ください)。深度6,000 mでは,圧力は600気圧,水温が2℃前後であり,この環境に二酸化炭素を注ぎ込むと,周りの海水と反応して勝手に二酸化炭素ハイドレートが生成します。この深さでは生成した二酸化炭素ハイドレートが液体の二酸化炭素より軽い(密度が小さい)ために,二酸化炭素ハイドレートがお鍋の「ふた」の役割を果たし,安定かつ海洋への二酸化炭素の溶解を最小限に食い止める貯蔵が可能となります。深さ3,000 mでも二酸化炭素ハイドレートは生成しますが,3,000 mでは液体の二酸化炭素の方が軽いため,液体二酸化炭素が直接海水と接触し,海洋へ二酸化炭素が溶解してしまい,広い範囲まで汚染が拡大する可能性が高くなります。 |

水 の密度(黒い線) 二酸化炭素の密度(青い線) 二酸化炭素ハイドレートの密度(赤い線) |
ガスをどのようにして輸送するのですか?
現在、日本は、天然ガスを液体にした液化天然ガス(LNG)の状態でLNGタンカーに積み、ガス田から天然ガスを運んでいます.
ところがこの方法だと、天然ガス(主成分のメタン)の液体になる温度が−160℃付近であるため、ものすごくコストがかかり,また、多くの無駄を発生します.そのため、すでにLNG方式で輸送しているところではなく、新規に開発される中小規模のガス田について、他にもっと経済的な方法がないかと検討されており,私たちの研究室で取り扱っているガスハイドレートを用いた輸送法もその一つです。
天然ガス(=メタンが主成分)を低温・高圧状態で水と反応させ天然ガスハイドレート(=NGH)としてタンカーで輸送するというものです。
■NGHとLNGの基礎物性値の違い(Nm3は0℃,1気圧換算)
| NGH (天然ガスハイドレート) | LNG (液化天然ガス) | |
| 輸送・貯蔵形態 | 固体 | 液体 |
| 保持温度 | −10℃ほど | −162℃ |
| 1m3中の成分 | 天然ガス165 Nm3 水0.8m3 | 天然ガス600 Nm3 |
ハイドレートを利用してガスを分離できるのですか?
ハイドレートは「かご」の中にゲスト分子を閉じこめて、成り立っています(ハイドレートについて詳しくはコチラ)。閉じこめることができる物質であっても、物質によって「かご」への入りやすさが異なります。しかも、「かご」にも大きさがあるため、全ての分子を閉じこめることができるわけではありません。水素分子は、分子のサイズが約0.3 nm(1 nmは1 cmの10000000分の1)とたいへん小さいため、極低温度や1000気圧以上の高圧力域でしか、ハイドレートを作らない分子です。
この性質を用いて、ハイドレートを作りやすい二酸化炭素などと水素が混合している気体の中で、ハイドレートを作ると二酸化炭素のみがハイドレートの「かご」の中にとりこまれて、固体の二酸化炭素(ハイドレート)と気体の水素に分離することが可能である。と考え、それに関する基礎研究を行っています。
我々は、様々なガスを水素に混ぜて、研究を行っています。その中でも、水素と二酸化炭素を混合した気体は、天然ガスから水素を作る「水蒸気改質」という過程で出てくる混合気体であり、水素を分離回収する重要な対象となります。現在、水素と二酸化炭素の混合した気体の吸着力の差(分離するためには何かの「差」が必要!!)を利用し分離するPressure Swing Adsorption法(PSA法)が主に用いられています。PSA法では高純度の水素が低圧力で回収できます。一方、ハイドレートを用いた分離では、ハイドレートを作るために高圧力が必要ですので、分離によって直接、高圧力の水素を回収することができます。
高圧力の水素使用の主な目的は、燃料電池自動車です。現在の燃料電池自動車は、約350気圧で圧縮水素ガスを載せて走っています。将来的には、約700気圧の水素を載せて走ることが想定されています。その際、水素供給スタンド(ガソリンスタンドのようなもの)には、さらに高圧力の1000気圧程度の水素が必要です。この水素供給スタンドで、ハイドレートが活躍できるのではないかと考えています。
ハイドレートに水素は貯蔵できないのですか?
水素ハイドレートは、極低温度や1000気圧以上の高圧力域でしか安定に存在できません。逆に言うと、これらの条件下では、水素を貯蔵することができると報告されています。貯蔵量は他の水素貯蔵媒体(水素吸蔵合金など)と比べて比較的大きい値であり、しかも、水素原子としてではなく、水素分子のまま貯蔵できるメリットがあります。しかし、実際に使用するとなると、温度は出来るだけ高く、圧力は出来るだけ低いことが重要になります。そこで、水素と水だけではなく、第三成分を加えることで、貯蔵量を幾分か犠牲にしても、圧力・温度をマイルドにすることが一つの可能性として考えられます。
世界中で、研究が盛んに行われており、もっとも有名な第三成分がテトラヒドロフランです。我々は、テトラヒドロフランを用いた場合の研究も行っていますが、それ以外に、臭化テトラブチルアンモニウムが第三成分として機能することを新たに発見しました。これらの第三成分を添加すると氷点以上の温度、数百気圧で水素貯蔵が可能です。現在、発見した第三成分を用いた系の相平衡測定、ラマン分光分析などによって、水素の貯蔵量を測定しています。また、貯蔵量・利用形態など総合的に優れた第三成分の探索を行っています。